作者: Eyal Hanania,
期刊/会议: Medical Image Analysis
年份: 2025
标签: T1 mapping Motion correction Myocardial imaging Deep learning Model-based deep learning Free-breathing MRI
核心贡献
- 实现了一种物理约束的,subject-specific self-supervise心脏磁共振定量以及配准网络。
- 前置工作PCMC-T1需要进行预训练,而MBSS-T1无需针对目标序列预训练,在每例数据上只需要6秒的优化,泛化能力更强。
Hanania E, Volovik I, Barkat L, et al. Pcmc-t1: Free-breathing myocardial t1 mapping with physically-constrained motion correction//International Conference on Medical Image Computing and Computer-Assisted Intervention. Cham: Springer Nature Switzerland, 2023: 226-235.
方法概述
模型可以分为两个子网络,如下图所示:
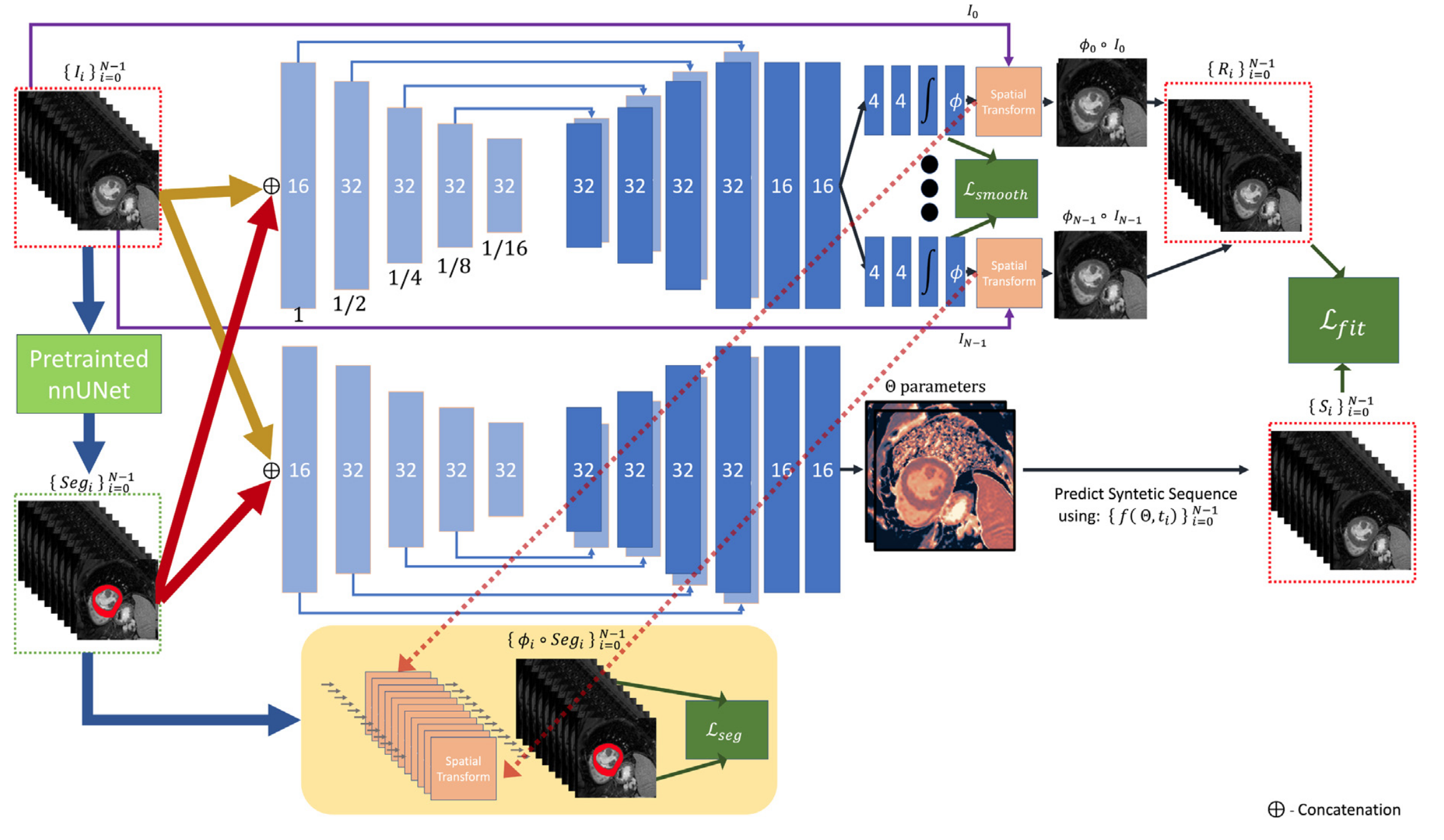
网络的输入是所有时刻的T1加权图像,以及这些图像的心肌分割mask。输出图像的变形场(用于运动矫正)和定量参数。
网络整体的目标函数可以表示为 $$ \Psi=\arg\min_{\psi}\sum_{i=0}^{N-1}\left\|f\left(NNmap_{\psi},t_i\right)-NNreg_{\psi}(i)\circ I_i\right\|^2 $$ 其中$NNmap_{\psi}$是网络输出的拟合参数,$NNreg_{\psi}(i)$是网络输出的第$i$张图像相对于参考图像的变形场,$I_i$是第$i$张T1加权图像($t_i$时刻的加权图像。
参考图像是在运动矫正过程中作为参考的图像,其他时刻的图像都向这张图像对齐,因此其变形场应该为恒定值(无变形)。参考图像选取分割结果中置信度最高的一张图。并且在其他分割结果中,也只取置信度较高的分割mask。
$NNmap_{\psi}$的拟合依据信号公式: $$ I(t)=A-B\cdot e^{-t/T1^*} $$ 其中$A,B,T1^*$为需要拟合的参数,$f\left(NNmap_{\psi},t_i\right)$是将拟合的参数根据信号公式[2]恢复成时间$t$的“模拟图像”。$NNreg_{\psi}(i)\circ I_i$是第$i$张运动矫正后的T1加权图。网络整体优化目标是使参数生成的模拟图像和运动矫正后的图像一致。理想状态下,如果运动矫正的完美的,则图像的每个pixel的$i$个点都应该符合公式[2]的信号公式。
网络整体的损失函数为: $$ \mathcal{L}_{total}=\lambda_1\cdot\mathcal{L}_{fit}+\lambda_2\cdot\mathcal{L}_{smooth}+\lambda_3\cdot\mathcal{L}_{Seg} $$ 其中匹配损失用于使运动矫正结果和信号公式生成的模拟图像一致: $$ \begin{aligned}\mathcal{L}_{fit}\left(\boldsymbol{\Theta},t_{i=0}^{N-1},\boldsymbol{\Phi}\right)&=\sum_{i=0}^{N-1}\left((S_i-R_i)\cdot K\right)^2\\&=\sum_{i=0}^{N-1}\left((f\left(\boldsymbol{\Theta},t_i\right)-\boldsymbol{\phi}_i\circ I_i)\cdot K\right)^2\end{aligned} $$ $K$表示分割得到的心肌mask,这里只计算心肌部分的匹配loss是因为心肌部分的信号是最符合公式[2]信号公式的,整体图像中包含的其他器官和背景部分可能不符合公式[2],从而对拟合造成干扰。
光滑损失通过限制变形场$\boldsymbol{\Phi}$的光滑来约束运动矫正符合心脏平缓的运动规律: $$ \mathcal{L}_{smooth}(\boldsymbol{\Phi})=\sum_{i=0}^{N-1}\frac{1}{\Omega}\sum_{p\in\Omega}\left\|\nabla\phi_i(p)\right\|^2. $$ 分割损失则约束运动矫正后的图像不仅在信号模型上对齐,也在解剖结构上对齐: $$ \mathcal{L}_{Seg}=\mathcal{L}_{MyoSeg}+\mathcal{L}_{LVSeg} $$ 分割损失同时计算了心肌和左心室(血池)部分分割mask的DiceLoss: $$ \mathcal{L}_{\mathrm{MyoSeg}}(r,\{MyoSeg_i\}_{i\in G},\{\phi_i\}_{i\in G})=\sum_{i\in G}\mathrm{DiceLoss}(MyoSeg_r,MyoSeg_i\circ\phi_i) $$
$$ \mathcal{L}_{\mathrm{LVSeg}}(r,\{LVSeg_i\}_{i\in G},\{\phi_i\}_{i\in G})=\sum_{i\in G}\mathrm{DiceLoss}(LVSeg_r,LVSeg_i\circ\phi_i) $$
这里计算的是参考图像和第$i$张图的Dice,与拟合参数生成的模拟图像无关。
实验设置
-
数据集:使用公开数据集https://cardiacmr.hms.harvard.edu/downloads-0,其中包含210例患有或疑似心血管疾病的MRI短轴图像,STONE序列,1.5T场强Philips Achieva采集,自由呼吸。
Weingärtner S, Roujol S, Akçakaya M, et al. Free‐breathing multislice native myocardial T1 mapping using the slice‐interleaved T1 (STONE) sequence. Magnetic resonance in medicine, 2015, 74(1): 115-124.
以及3T场强Siemens PRISMA采集的私有数据集,使用MOLLI序列,19例患者,每例患者采集5层,FOV $306 \times 360 mm^2$,FA 35°,层厚 8mm。分别采集自由呼吸和屏气状态下的数据。数据采集过程中不使用呼吸导航,并且额外重新采集了5例患者的数据用于再测信度分析。
-
对比方法:共进行了三组实验,第一组在STONE公开数据集上和对比方法进行比较,这里的对比方法有Reg-MI,SynthMorph,Voxelmorph-seg,PCMC-T1,和无运动矫正直接拟合
Hoffmann M, Billot B, Greve D N, et al. SynthMorph: learning contrast-invariant registration without acquired images. IEEE transactions on medical imaging, 2021, 41(3): 543-558.
Balakrishnan G, Zhao A, Sabuncu M R, et al. Voxelmorph: a learning framework for deformable medical image registration. IEEE transactions on medical imaging, 2019, 38(8): 1788-1800.
Hanania E, Barkat L, Cohen I, et al. Deep-learning-based group-wise motion correction for myocardial T1 mapping//Proceedings of the ISMRM & SMRT Annual Meeting & Exhibition, Toronto, Canada. 2023.
Hanania E, Volovik I, Barkat L, et al. Pcmc-t1: Free-breathing myocardial t1 mapping with physically-constrained motion correction//International Conference on Medical Image Computing and Computer-Assisted Intervention. Cham: Springer Nature Switzerland, 2023: 226-235.
第二组在MOLLI序列采集的屏气自由呼吸数据上进行比较,对比方法有无运动矫正直接拟合,Siemens MyoMap(扫描仪自带)和SynthMorph。
Xue H, Shah S, Greiser A, et al. Motion correction for myocardial T1 mapping using image registration with synthetic image estimation. Magnetic resonance in medicine, 2012, 67(6): 1644-1655.
第三组实验主要用于再测信度分析,不评估配准质量,而是评估重复测量的ICC一致性,对比方法是无运动矫正和Siemens MyoMap。
-
评价指标:实验一和二的评价指标是:$R^2$,DSC,HD,医学主观评分
其中$R^2$的公式是: $$ R^2 = 1 - \frac{\sum_{i=0}^{N-1}(y_i - \hat{y}_i)^2}{\sum_{i=0}^{N-1}(y_i - \bar{y})^2} $$ 用于评价拟合优度,也就是不同TI时间的图像有多符合信号公式[2]
DSC和HD都是通过检验配准后不同TI图像心肌mask的一致性来判断配准的准确度。主观评分用于判断配准后图像在医疗中的贡献度。
实验三的指标是ICC,用于衡量多次测量结果的一致性,ICC取值在0-1之间,越接近1说明重复测量高度一致,方法越可靠。文中采用的是ICC3,其公式为: $$ ICC3=\frac{MS_R-MS_E}{MS_R+(k-1)MS_E} $$ 其中:$MS_R=\frac{SS_R}{n-1}$,$MS_E=\frac{SS_E}{(n-1)(k-1)}$,n表示受试者数量,k表示重复测量次数,$MS_R$表示受试者间均方,$MS_E$表示误差均方,$SS$表示平方和。分子部分表示受试者间的差异,分母部分表示总差异,其比值越大说明总体差异中的大部分来自于个体差异而非重复测量误差,说明测量一致性越高。
Koo T K, Li M Y. A guideline of selecting and reporting intraclass correlation coefficients for reliability research. Journal of chiropractic medicine, 2016, 15(2): 155-163.
https://zhuanlan.zhihu.com/p/599576232
结果分析
在前两项实验中,所提方法在所有指标上都表现更好
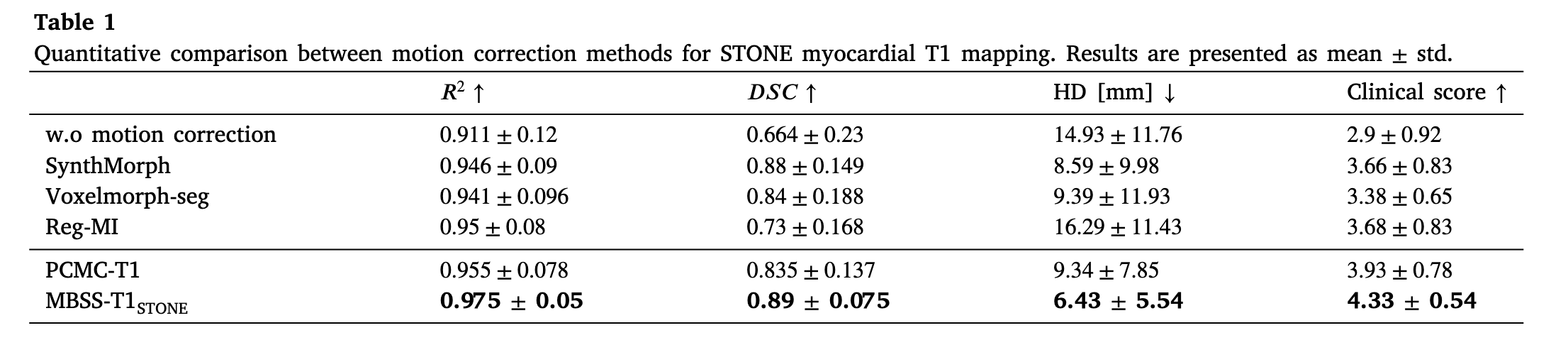
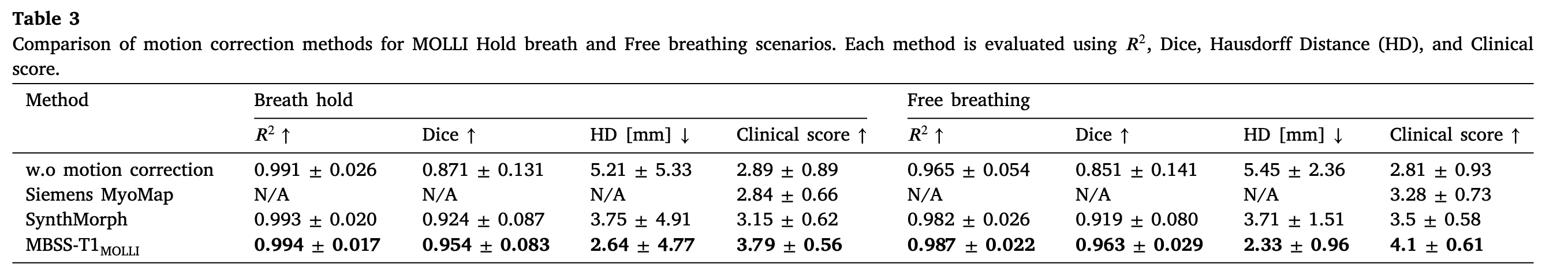
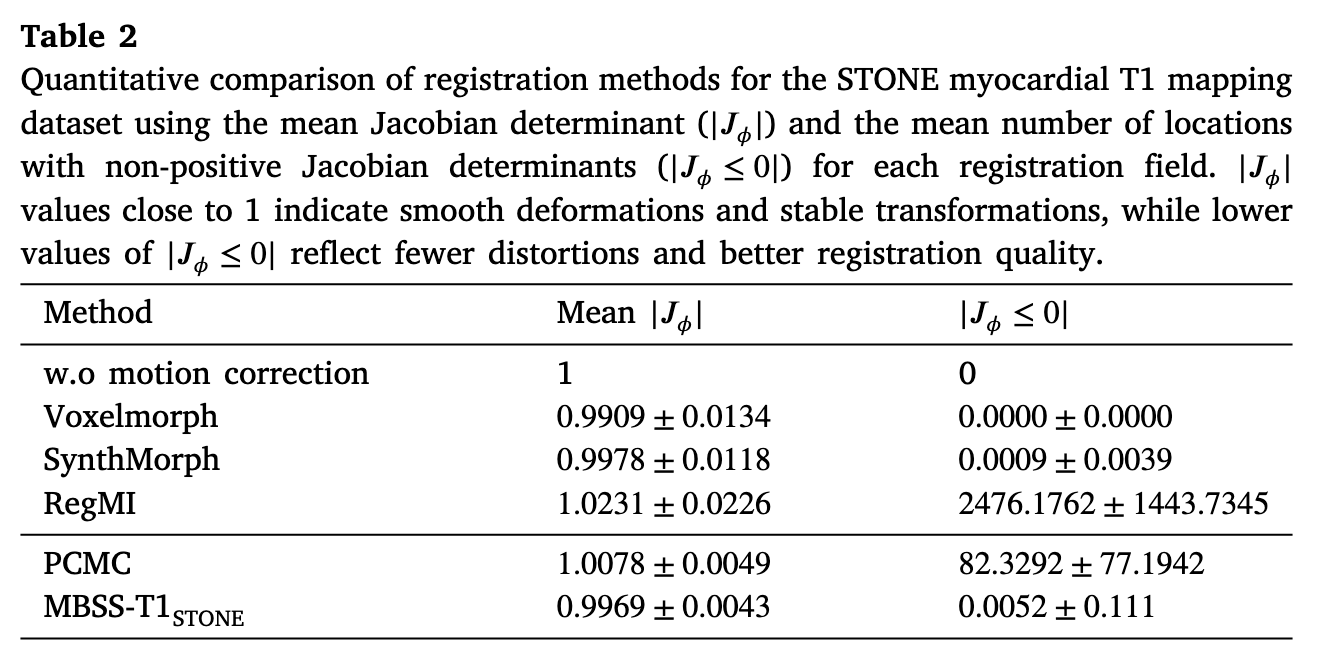
对于第一项实验,还额外计算了变形场的Jacobian行列式$|J_\phi|$来评估变形场质量。心脏的运动应该是平滑的,因此不应该出现$|J_\phi|\leq0$的情况,因为这种情况表示变形场出现了折叠。而理想情况应该是$|J_\phi|=1$表示局部没有出现膨胀或者压缩,而是平滑变形。因此原文中的Table2中有两个指标,$mean|J_\phi|$越接近1说明变形越平滑,$|J_\phi\leq0|$数量越少说明不合理变形的点越少。
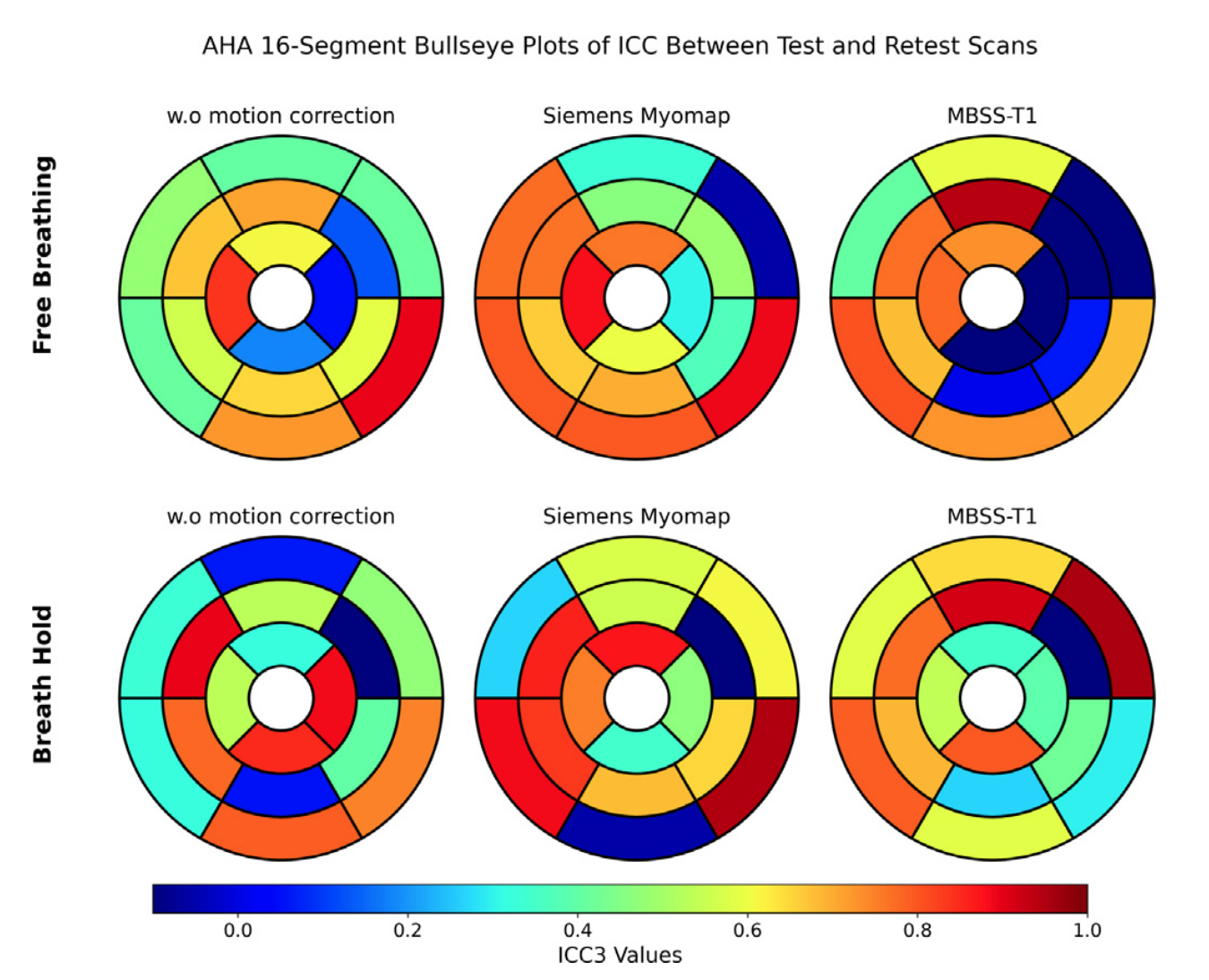
实验三的ICC的平均是MBSS-T1最低,但是在AHA16段图中,没有哪个方法在每个分割区域中都更好。
个人思考
- 可借鉴的点:使用$R^2$作为指标来判断拟合的准确程度;使用ICC3作为指标来判断方法的可重复性
- 存在的问题:对于拟合的准确程度是通过$R^2$和主观打分来判断的,而没有通过例如水膜或者IR-SE采集的图像来判断T1map是否准确
- 与我研究的关联:
- 我的理解程度:
⭐️⭐️⭐️⭐️(没有复现代码)